4月17日,中国科学院上海营养与健康研究所李虹研究团队在国际学术期刊Cell Reports Medicine在线发表了题为“Pan-cancer analysis of spatial transcriptomics reveals heterogeneous tumor spatial microenvironment”的研究论文。该研究定义了泛癌中保守且核心的空间生态位,系统解析了泛癌空间微环境的复杂性、不同癌种的共性规律与独特模式,并阐明了生态位相关的分子特征,及其与患者预后和免疫治疗响应的关联。
肿瘤是由肿瘤细胞、基质细胞及免疫细胞共同构成的复杂的生态系统,其相互作用构建的肿瘤微环境在肿瘤发生、进展、侵袭与转移中均具有关键作用。李虹研究组多年来在肿瘤微环境解析方向持续深耕,全面阐述了不同尺度空间特征的计算方法(NPJ Precis Oncol 2025, 9(1):68),开发了对微环境空间结构进行综合分析的工具包(Genome Biol 2025,26(1):80)。结合单细胞空间图谱计算解析与实验验证,阐明了肝癌成纤维细胞的表达异质性、功能多样性、空间分布和细胞间通讯(Genome Med 2024, 16(1):98);刻画了胆囊癌发生多阶段的细胞命运重塑特征并发现了PRDX1+巨噬细胞显著抑制胆囊癌恶性表型(Int J Surg 2026,doi:10.1097/JS9.0000000000004916);鉴定出胰腺癌肝转移高度相关的恶性细胞亚群并证实了靶向其特征基因H2AFZ可显著抑制肝转移形成(Clin Cancer Res 2026,doi: 10.1158/1078-0432)。然而,当前空间组学研究普遍存在样本规模有限的问题,且多集中于单一癌种或特定细胞类型。随着空间组学数据的不断积累,系统解析跨癌种肿瘤空间微环境特征已成为亟待解决的重要问题。
受癌种、数据集及样本间异质性影响,泛癌空间转录组数据的整合分析在计算层面具有较高挑战性。该研究针对泛癌异质性和分析目标设计并优化了空间转录组整合分析策略,从空间生态位、细胞互作、分子特征及临床意义多个层面,系统解析了泛癌肿瘤空间微环境的共性规律(图1)。通过对12种癌种的373例样本开展泛癌空间转录组分析,在不同的空间尺度上定义了56个局部细胞组成(Local cellular programs)和13个空间生态位(Niche),这些生态位是泛癌中保守且基础的空间结构单元。单个样本内普遍存在多个生态位,反映了肿瘤内部空间微环境的多样性;基于生态位组成的样本聚类分析进一步揭示了肿瘤间异质性,各聚类均包含多种癌种,但部分肿瘤类型对特定聚类呈现出明显的偏好。
为进一步探究这些生态位的内在机制,研究人员对生态位相关的配体-受体(LR)相互作用及细胞类型特异性基因表达进行了分析,发现了不同生态位间共有的或特有的LR相互作用,且部分LR表达与患者预后显著相关,提示LR介导的细胞互作与生态位形成及其功能密切相关。细胞类型特异性差异表达分析显示,特定细胞类型的基因表达在不同生态位间存在显著差异,反映了细胞转录谱与其局部微环境的密切关联。
联合分析11种癌种5162例患者、8个免疫治疗队列776例患者的bulk转录组数据,发现多个生态位与患者预后及免疫治疗响应显著相关。Niche_13生态位为免疫热型,富含抗肿瘤免疫细胞,对免疫治疗敏感;Niche_4为肿瘤-巨噬细胞共定位的免疫抑制型微环境,与不良预后及免疫治疗耐药相关;而与其它免疫细胞共定位的巨噬细胞(Niche_11)则预示着更好的生存获益与免疫治疗响应。巨噬细胞的空间分布模式及其双重作用,是预测患者预后及免疫治疗响应的潜在生物标志物,未来具有临床转化潜力。
综上,该研究综合使用了空间转录组、单细胞转录组、bulk转录组和多通道蛋白成像数据对肿瘤空间微环境进行系统解析,为理解复杂肿瘤生态系统中的细胞间空间关系与相互作用机制提供了更深刻的见解。
中国科学院上海营养与健康研究所李虹研究员为该论文通讯作者,博士研究生李家荣为该论文第一作者。该工作得到国家卫健委四大慢病重大项目、国家自然科学基金项目、上海市级科技重大专项等项目的资助。研究使用的所有组学数据均来自公开发表的数据集。
原文链接:https://doi.org/10.1016/j.xcrm.2026.102751
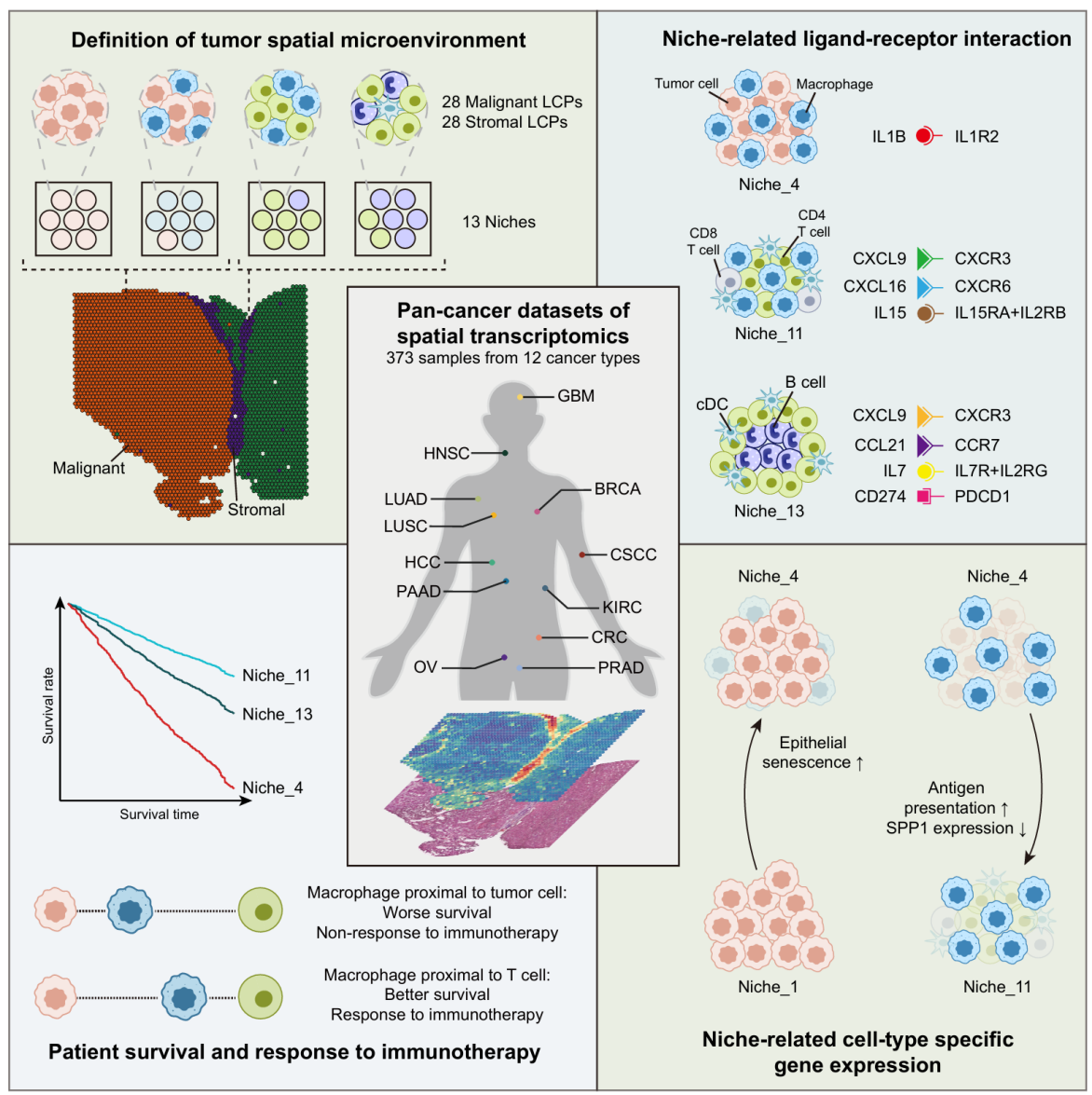
图:泛癌空间微环境解析策略与结果概览图
推送单元:李虹研究组、科技规划与任务处