4月4日,中国科学院上海营养与健康研究所应浩研究组在Oncogene期刊在线发表了标题为“Deciphering functional intra-tumoral heterogeneity in BRAFV600E-driven mouse thyroid cancer reveals EMT trajectory and metabolic remodeling”的研究论文。该研究揭示了BRAFV600E突变的甲状腺肿瘤细胞存在多个具有不同程度间质转化与稳定性的细胞亚群,恶性细胞亚群沿上皮-间充质转化(EMT)轨迹由中间状态逐步向更具间质与恶性的状态推进。
甲状腺乳头状癌(Papillary thyroid cancer, PTC)是最常见的内分泌恶性肿瘤之一,起源于甲状腺滤泡上皮细胞的恶性转化。尽管PTC通常预后良好,但其转移十分常见,其中微转移更为普遍,发生率接近90%。PTC的转移与其持续存在及复发显著相关。因此,深入理解肿瘤内部的功能异质性,将有助于改进分子诊断策略,并推动针对PTC患者的有效治疗方法的研发。
研究团队利用由BRAFV600E突变驱动的成年发病型原位PTC小鼠模型以及单细胞RNA测序技术,探讨了恶性甲状腺肿瘤细胞的转录异质性和细胞层级结构,并鉴定出处于不同细胞状态的多个细胞亚群,这些亚群具有不同程度的稳定性和EMT特征,排列形成一条单一而非分叉的EMT演化轨迹。细胞沿该轨迹经历中间状态并最终转变为更具恶性的细胞状态。基于流式分选技术和类器官培养体系,研究团队获取了不同的恶性细胞亚群,并验证其功能异质性和细胞状态转换。此外,研究团队发现二甲双胍治疗可抑制PTC肿瘤发生,并减少最具恶性的细胞亚群。通过类器官培养,证明二甲双胍能够抑制EMT过程,提示其具有作为针对BRAFV600E突变驱动的PTC治疗干预手段的潜力。
通过整合癌症基因组图谱(TCGA)数据以及人类患者的单细胞RNA测序数据,研究团队发现本研究所鉴定的肿瘤内异质性特征以及功能性状态具有临床相关性,其中一个与EMT轨迹相关的基因模块对携带BRAFV600E突变的人类PTC具有重要诊断价值。
最后,该研究还表明,p53缺失可能降低了BRAFV600E突变驱动肿瘤发生的阈值,并促进细胞状态向更具恶性的方向转变,但并不影响异质性或演化轨迹本身。在机制上,p53缺失可能通过增强线粒体氧化磷酸化来调节代谢可塑性,从而赋予BRAFV600E突变的甲状腺细胞更强的恶性潜能,这一机制对转移具有重要功能意义,揭示了主要致癌基因驱动与次级遗传损伤在塑造肿瘤代谢中的协同作用,提示线粒体氧化磷酸化可作为晚期疾病的潜在治疗靶点。
综上,研究不仅解析了BRAFV600E突变驱动的PTC的肿瘤内功能异质性,也为开发靶向EMT或代谢途径的治疗策略提供了理论基础。
中国科学院上海营养与健康研究所于靖和沈思艺博士为该论文的共同第一作者,应浩研究员、沈思艺博士以及上海交通大学医学院附属第九人民医院张凌副主任医师为该论文的共同通讯作者。该研究得到了上海市东方英才计划(领军)、上海市超级博士后激励计划、以及上海市自然科学基金等项目的资助,同时也得到了中国科学院上海营养与健康研究所所级公共技术中心的支持。研究使用的人体组学数据均来自公开发表的数据集。
原文链接:https://doi.org/10.1038/s41388-026-03742-8
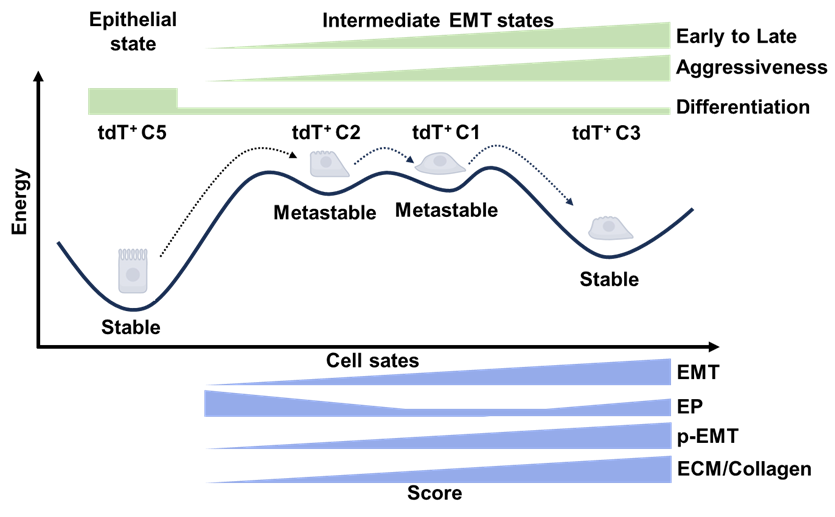
图:BRAFV600E突变驱动的小鼠PTC中各亚群的不同细胞状态和转变轨迹
推送单元:应浩研究组、科技规划与任务处