11月5日,中国科学院上海营养与健康研究所邵振研究组在Nature Communications发表研究论文:Transcription factor ZNF263 primes human embryonic stem cells for pluripotency dissolution and lineage commitment。该研究结合大规模计算生物学筛选分析和一系列功能实验,揭示了锌指转录因子ZNF263在调控人胚胎干细胞始发多能态建立维持、多能性融解直至胚层分化命运决定这一连续动态过程中的关键作用。
研究人员首先搜集了大量不同人类细胞类型和状态的表观基因组数据,并应用前期开发的MAmotif工具包进行大规模计算生物学筛选,发现ZNF263结合motif显著富集在始发态人胚胎干细胞中特异性激活的基因启动子上,暗示它很可能在人类多能性调控网络中扮演某种重要角色。
然后,研究人员通过ChIP-seq实验证实,ZNF263在人胚胎干细胞中广泛结合多能性维持和干细胞分化相关基因的启动子,形成一个独立于POU5F1(OCT4)、SOX2和NANOG等核心多能性因子的调控模块,暗示它可能有不同的多能性调控作用。研究团队进一步构建了ZNF263敲除的人胚胎干细胞系,发现ZNF263缺失后,碱性磷酸酶活性等多能性标志物和PRDM14等原始多能态相关基因表达上调,而ZIC2等早期分化因子表达下调,暗示始发多能态相关的基因表达平衡受到破坏。更深入的机制分析表明,在人胚胎干细胞中,ZNF263通过直接调控ZIC2的表达和染色质结合,进而建立以ZNF263-ZIC2轴为核心的正前馈回路,驱动基因表达程序从多能性维持向谱系分化偏移,使细胞为多能性退出和胚层分化命运决定做好准备。
最后,研究人员指出ZNF263缺失后,人胚胎干细胞多能性退出过程的效率显著降低,向三个胚层特别是外胚层分化的能力受到明显损害。单细胞转录组分析则指出,野生型始发态人胚胎干细胞中,存在两个分别表现出较高中内胚层和外胚层分化倾向的细胞亚群;而ZNF263缺失后,这些高谱系分化倾向的细胞比例显著降低。
上述研究系统揭示了ZNF263在人胚胎干细胞中,通过调控多能性维持与谱系分化两方面基因之间的表达平衡,主导了始发多能态基因表达程序的建立和维持,并进一步助推后续多能性退出和胚层分化过程。其与ZIC2等早期发育因子之间的协同作用以及与Wnt等关键发育信号通路的互作,有可能为进一步理解人类细胞多能性状态转换和早期胚胎发育的分子调控机制提供新的线索。
营养与健康所副研究员尹倩倩、博士后黄静、博士毕业生孙洪铎、研究生周书晗为该论文共同第一作者,研究员邵振为通讯作者。该研究受到国家科技部、国家自然科学基金委员会、中国科学院等基金的资助。
论文链接:https://www.nature.com/articles/s41467-025-64290-5
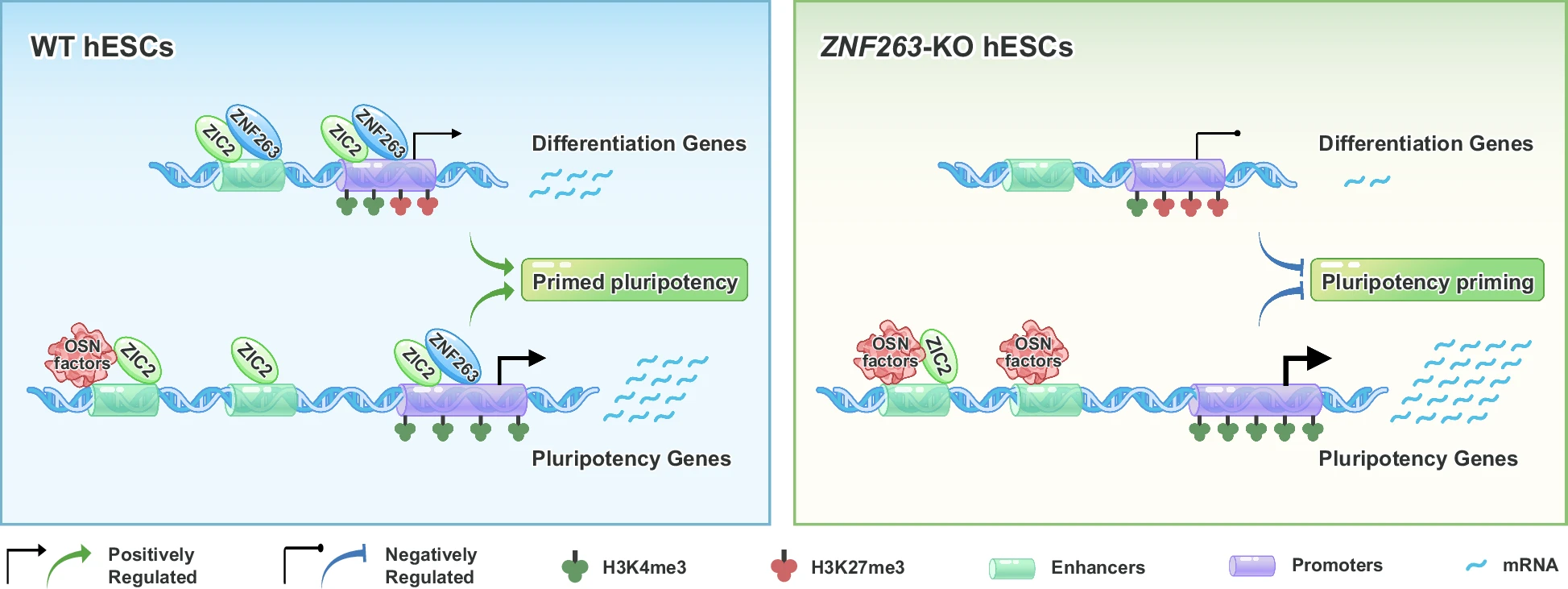
图:在人胚胎干细胞中,ZNF263通过以ZNF263-ZIC2轴为核心的正前馈回路,驱动了始发多能态转录程序的建立
推送单元:邵振研究组、科技规划与任务处